Την τελευταία δεκαετία, η έννοια της ιατρικής ακριβείας στην ογκολογία έχει αναδειχθεί ως μια καινοτόμος προσέγγιση που βασίζεται στην ικανότητα προσδιορισμού αλληλουχίας του γονιδιώματος (DNA) των καρκινικών κυττάρου της νεοπλασίας του κάθε ασθενή. Τα στοχευμένα φάρμακα αποσκοπούν στη βελτιστοποίηση των θεραπειών και στην κατανόηση της δυναμικής εξέλιξης του καρκίνου σε μία εποχή που οι προσδοκίες για νέες και αποτελεσματικές θεραπείες είναι μεγαλύτερες από ποτέ.
Η βιοψία ιστού είναι σήμερα η τυπική μέθοδος για τη διάγνωση και τον μοριακό χαρακτηρισμό των όγκων. Ωστόσο, έχει πολλούς περιορισμούς λόγω της επεμβατικότητάς της ως διαδικασία, καθώς και των πιθανών επιπλοκών αυτής όπως αιμορραγία, τραυματισμός, μόλυνση, πόνος. Άλλοτε πάλι η προσβασιμότητα στον ιστό για βιοψία είναι περιορισμένη και η επάρκεια ή η ποιότητα του δείγματος είναι ακατάλληλες για περεταίρω χειρισμούς. Σε αυτό το πλαίσιο, η « υγρή βιοψία » απέδειξε γρήγορα τη χρησιμότητά της ως μία μη επεμβατική, εύκολα επαναλαμβανόμενη διαγνωστική εξέταση, ικανή να προσδιορίσει το μοριακό προφίλ κάθε όγκου και να καθοδηγήσει την κλινική διαχείριση ασθενών με καρκίνο.
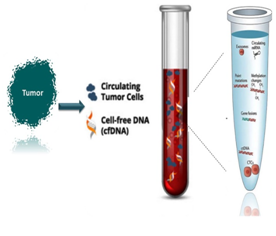
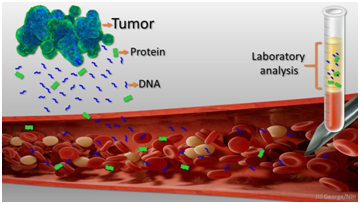
Ο όρος υγρή βιοψία αναφέρεται στην εξέταση βιολογικών υγρών μέσω κυτταρικών και μοριακών τεχνικών προκειμένου να αντληθούν πληροφορίες σχετικά με τη βιολογία και τη δυναμική του καρκινικού κυττάρου. Η πιο ευρέως εξεταζόμενη και πιο συχνά χρησιμοποιούμενη αναλυόμενη ουσία είναι σίγουρα το αίμα. Ωστόσο, οι υγρές βιοψίες έχουν επίσης διερευνηθεί (με πολλά υποσχόμενα αποτελέσματα) σε ένα ευρύ φάσμα εναλλακτικών (περισσότερο ή λιγότερο εύκολα προσβάσιμων) σωματικών υγρών, συμπεριλαμβανομένων των ούρων, της υπεζωκοτικής συλλογής, της ασκιτικής συλλογής, του εγκεφαλονωτιαίου υγρού και του σάλιου.
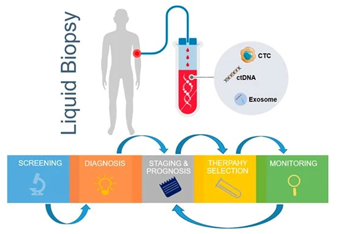
Η ογκολογική κοινότητα ορίζει την υγρή βιοψία ως μια εξέταση που γίνεται σε δείγμα αίματος για την αναζήτηση καρκινικών κυττάρων που κυκλοφορούν στο αίμα ή για τμήματα DNA από καρκινικά κύτταρα που βρίσκονται σε αυτό. Η υγρή βιοψία μπορεί να χρησιμοποιηθεί για να βοηθήσει στην ανεύρεση του καρκίνου σε πρώιμο στάδιο, να συνδράμει στον προγραμματισμό της θεραπείας, να διαπιστώσει πόσο καλά λειτουργεί η θεραπεία ή εάν ο καρκίνος έχει επανεμφανιστεί ή και υποτροπιάσει. Η δυνατότητα λήψης πολλαπλών δειγμάτων αίματος με την πάροδο του χρόνου στον ίδιο ασθενή μπορεί επίσης να βοηθήσει τους γιατρούς να καταλάβουν τι είδους μοριακές αλλαγές συμβαίνουν σε έναν όγκο υπό την επίδραση των θεραπειών.
Βιοδείκτες υγρής βιοψίας
Τα τελευταία χρόνια έχουν ανακαλυφθεί διαφορετικοί βιοδείκτες για την διενέργεια και την αξιολόγηση της υγρής βιοψίας προσφέροντας διάφορους τύπους πληροφοριών. Οι πιο συχνά χρησιμοποιούμενες προσεγγίσεις περιλαμβάνουν την ανάλυση των ελεύθερων κυττάρων – cell free DNA (cfDNA) και του κυκλοφορούντος DNA όγκου – circulating DNA (ctDNΑ), με το τελευταίο να είναι αυτό που έχει αναδειχθεί ως το πιο υποσχόμενο και να εμφανίζεται στις περισσότερες των περιπτώσεων.
Το μικροπεριβάλλον του όγκου περιλαμβάνει ένα μείγμα κυτταρικών και μη κυτταρικών συστατικών, πολλά από τα οποία απελευθερώνονται από τα καρκινικά κύτταρα, τα οποία συμβάλλουν στην επιβίωση του καρκίνου, την εισβολή, τη μεταστατική διαδικασία και την αντίσταση στις θεραπείες. Μεταξύ αυτών των συστατικών, τα ctDNA και cfDNA ξεχώρισαν για τα χαρακτηριστικά τους ως χρήσιμοι βιοδείκτες που κυκλοφορούν στο περιφερικό αίμα ασθενών με καρκίνο.
Κλινικές εφαρμογές υγρής βιοψίας στην ογκολογική πρακτική
Προσυμπτωματικός έλεγχος καρκίνου και έγκαιρη ανίχνευσή του
Μία από τις εφαρμογές υψηλού ενδιαφέροντος της υγρής βιοψίας είναι ο προσυμπτωματικός έλεγχος και η έγκαιρη ανίχνευση καρκίνου σε ασυμπτωματικούς πληθυσμούς. Η ανίχνευση του καρκίνου σε πρώιμο στάδιο, σε περιπτώσεις δηλαδή που αυτός μπορεί να είναι πλήρως ιάσιμος, μπορεί να συμβάλει στη μείωση της ογκολογικής θνησιμότητας. Ένα αξιόπιστο εργαλείο υγρής βιοψίας σε επίπεδο προσυμπτωματικού ελέγχου θα απαιτούσε υψηλά εξειδικευμένη μεθοδολογία σε συνδυασμό με κλινικά σημαντική ευαισθησία και θα ταξινομούσε ιδανικά τον ιστό προέλευσης. Καθώς οι καρκίνοι πρώιμου σταδίου είναι γνωστό ότι εκκρίνουν χαμηλότερα επίπεδα ctDNA σε σύγκριση με τη μεταστατική νόσο, σε αυτή τη ρύθμιση πρέπει να χρησιμοποιηθούν εξειδικευμένες αναλύσεις με υψηλή ευαισθησία και ικανότητα ανίχνευσης πολύ χαμηλών επιπέδων ctDNA. Σε αυτό το πλαίσιο έχουν διερευνηθεί αρκετές μεθοδολογικές προσεγγίσεις που δίνουν πολλά υποσχόμενα αποτελέσματα για το μέλλον.
Αρχική διάγνωση και γονότυπος του καρκίνου, σε πρώιμο ή προχωρημένο στάδιο
Στις περισσότερες περιπτώσεις, μια υποψία καρκινικής βλάβης στην απεικόνιση επιβεβαιώνεται με ιστική βιοψία αυτής. Ωστόσο, η ταυτοποίηση παθογνωμονικών μεταλλάξεων στο ctDNA μπορεί να βοηθήσει στην αρχική διάγνωση του καρκίνου και στον προσδιορισμό του γονότυπου αυτού σε ασθενείς με όγκους που είναι δύσκολο να ληφθεί βιοψία ή ασθενείς με αντενδείξεις για δειγματοληψία ιστού. Σύμφωνα με τις τελευταίες κατευθυντήριες οδηγίες, συστήνεται η ανάλυση ctDNA για προχωρημένες νεοπλασίες συμπαγών οργάνων σε περιπτώσεις όπου η ανάλυση ιστού δεν είναι δυνατή. Σε περίπτωση αρνητικών αποτελεσμάτων υγρής βιοψίας, η πιθανότητα ψευδώς αρνητικών πρέπει να λαμβάνεται υπόψη και να καθοδηγείται η περαιτέρω διαχείριση του ασθενούς σε εξατομικευμένη βάση.
Πρόγνωση
Η ανίχνευση υπολειπόμενου κυκλοφορούντος ctDNA (που δηλώνει μικροσκοπικά υπολειπόμενη νόσο) πριν αλλά κυρίως μετά το τέλος μίας θεραπείας, έχει αποδειχθεί σε μελέτες ότι έχει αρνητική προγνωστική αξία και έχει συνδεθεί με υψηλό κίνδυνο υποτροπής σε ασθενείς με καρκίνο πρώιμου σταδίου. Οι προγνωστικοί παράγοντες χειρότερης έκβασης περιλαμβάνουν τα ακόλουθα: ταύτιση του ctDNA σε ιστό και υγρή βιοψία, αυξημένα επίπεδα κυκλοφορούντος ctDNA και υψηλά ποσοστά μεταλλαγών αυτού.
Παρακολούθηση μοριακής υποτροπής
Μια άλλη κλινική εφαρμογή που παρουσιάζει ιδιαίτερο ενδιαφέρον στον καρκίνο πρώιμου σταδίου είναι η ποσοτική ανίχνευση του ctDNA κατά τη διάρκεια της παρακολούθησης ασθενών σε φάση κλινικής πλήρους ύφεσης χωρίς κάποια μακροσκοπική ένδειξη επανεμφάνισης της ασθένειας μετά από ριζική θεραπεία. Η προγνωστική αξία της ανίχνευσης ctDNA κατά τη διάρκεια της παρακολούθησης έχει αποδειχθεί σε αρκετές μελέτες. Ωστόσο, με ποιο τρόπο η «υποτροπή ctDNA» θα μπορούσε να επηρεάσει ουσιαστικά τη διαχείριση του ασθενούς παραμένει ασαφές. Για παράδειγμα, η έγκαιρη ανίχνευση του ctDNA θα μπορούσε ενδεχομένως να προκαλέσει στενότερη παρακολούθηση μέσω κλινικών και απεικονιστικών αξιολογήσεων προκειμένου να ανιχνευθεί νωρίτερα η ακτινολογική υποτροπή, όταν ο όγκος μπορεί ακόμη να υποβληθεί σε ριζική θεραπεία.
Αξιολόγηση στοχευόμενων μεταλλάξεων
Αν και το τυπικό γονιδιωματικό προφίλ για την ανίχνευση στοχευόμενων αλλοιώσεων εξακολουθεί να περιλαμβάνει δοκιμές με βάση τον ιστό, πολυάριθμες προοπτικές και αναδρομικές μελέτες έχουν αποδείξει υψηλή ειδικότητα και θετικά προγνωστικά αποτελέσματα, που κυμαίνονται από 95% έως 99%, όταν συγκρίνονται τα αποτελέσματα υγρής βιοψίας ctDNA με αυτά που λαμβάνονται μέσω ιστικών βιοψιών σε προχωρημένους όγκους. Ως εκ τούτου, η εφαρμογή της σε αυτό το κλινικό περιβάλλον έχει θεωρηθεί πολύτιμη και οδήγησε στην έγκριση αρκετών μελετών ανάλυσης της αποτελεσματικότητας στοχευμένων θεραπειών ακόμα και σε περιπτώσεις καρκίνου αγνώστου πρωτοπαθούς εστίας και προέλευσης.
Εκτίμηση της ανταπόκρισης και πρόβλεψη του αποτελέσματος της ανοσοθεραπείας
Η ανταπόκριση στην ανοσοθεραπεία έχει αποδειχθεί ότι σχετίζεται με το συνολικό φορτίο μεταλλαγών (TMΒ) και την υψηλή μικροδορυφορική αστάθεια (MSI) που ανιχνεύονται με βάση την ιστική προσέγγιση του όγκου. Έχουν πραγματοποιηθεί αρκετές μελέτες για την αξιολόγηση της συσχέτισης των ιστικών ΤMB και MSI σε σχέση με τα αντίστοιχα που προέρχονται από το αίμα. Στη σύγχρονη ογκολογία απαιτούνται πρώιμες εκτιμήσεις της δράσης της ανοσοθεραπείας στην κλινική πρακτική προκειμένου να αξιολογηθεί καλύτερα η ανταπόκριση του όγκου. Ειδικά η ψευδο-πρόοδος, η αρχική δηλαδή αύξηση του μεγέθους του όγκου στις απεικονίσεις που πιθανώς τροφοδοτείται από φλεγμονή λόγω υπερδιέγερσης του ανοσοποιητικού, μπορεί συχνά να ανιχνευθεί στην αρχή της χορήγησης της ανοσοθεραπείας, παρά την εικόνα συνολικής κλινικής ανταπόκρισης του ασθενούς. Ως εκ τούτου, το cfDNA/ctDNA έχει εξεταστεί ως ένα πιθανό εργαλείο για την αξιολόγηση της ανταπόκρισης στην ανοσοθεραπεία σε αρκετές δοκιμές.
Επαναλαμβανόμενη δειγματοληψία για παρακολούθηση της ανταπόκρισης σε στοχευμένη θεραπεία και χημειοθεραπεία
Εκτός από την ανοσοθεραπεία, κρίνονται απαραίτητα επίσης τα πρόσθετα εργαλεία για την αξιολόγηση της ανταπόκρισης στη θεραπεία σε ασθενείς που λαμβάνουν στοχευμένη θεραπεία ή χημειοθεραπεία. Ως εκ τούτου, αρκετές μελέτες έχουν αναλύσει τη χρήση ctDNA σε αυτό το πλαίσιο. Αν και οι παραδοσιακοί καρκινικοί δείκτες βρίσκουν ευρεία εφαρμογή για την παρακολούθηση θεραπευτικής ανταπόκρισης στην τρέχουσα κλινική πρακτική, το ctDNA έχει αποδειχθεί ότι είναι ανώτερο και σαφώς πιο αξιόπιστο σε αυτό το πλαίσιο.
Ανίχνευση μηχανισμών αντίστασης στη συστηματική θεραπεία
Ένα άλλο σημαντικό πεδίο ενδιαφέροντος στην εφαρμογή του ctDNA είναι η πιθανή ανίχνευση του μηχανισμού αντίστασης που αναπτύσσεται υπό μία συστηματική θεραπεία. Η ανάλυση ctDNA του πλάσματος επιτρέπει την παρακολούθηση διαφόρων μηχανισμών αντίστασης στη στοχευμένη θεραπεία. Αυτοί οι μηχανισμοί αντίστασης περιλαμβάνουν συν-μεταλλάξεις που εμφανίζονται κατά τη διάρκεια της θεραπείας και μπορούν να επηρεάσουν τις θεραπευτικές αποφάσεις σε πολλαπλούς τύπους καρκίνου, με ιδιαίτερη εφαρμογή να παρατηρείται σε ασθενείς με μη μικροκυτταρικό καρκίνο του πνεύμονα και καρκίνο του παχέος εντέρου. Εκτός από την αξιολόγηση των γνωστών μηχανισμών αντοχής, η ανίχνευση άγνωστων μηχανισμών μέσω του cfDNA έχει μελετηθεί σε αρκετές δοκιμές, είτε με τη χρήση μεγάλων πάνελ μοριακών μεταλλάξεων, είτε με στοχευμένη προσέγγιση σε περιπτώσεις όπου είναι γνωστή κάποια πιθανή συσχέτιση με αντοχή σε μια συγκεκριμένη θεραπεία.
Αξιολόγηση ctDNA που προέρχονται από πολλαπλές μεταστατικές θέσεις και ετερογένεια όγκου
Η ετερογένεια των καρκινικών κυττάρων, ειδικά στο μεταστατικό περιβάλλον, μπορεί να παίξει σημαντικό ρόλο στις θεραπευτικές προσεγγίσεις. Τα δείγματα όγκου που προέρχονται από ιστούς, μπορούν να παρέχουν την αξιολόγηση μιας περιορισμένης ποσότητας συγκεκριμένου νεοπλασματικού υλικού σε ένα δεδομένο χρονικό σημείο. Οι υγρές βιοψίες θα μπορούσαν να λειτουργήσουν ως επιπρόσθετο εργαλείο για τη συμπλήρωση του γενετικού ογκολογικού τοπίου, καθώς το ctDNA μπορεί να προέρχεται εκκρινόμενο στο αίμα από διαφορετικά σημεία του όγκου (πιθανώς ετερογενή μεταξύ τους) ή των μεταστάσεων αυτού, πληροφορίες που μπορούν να αξιολογηθούν συνδυαστικά κατά βούληση.
Μελλοντικές προοπτικές
Συμπερασματικά, η υγρή βιοψία υπόσχεται πολλά στην έρευνα και τη διάγνωση του καρκίνου. Προσφέρει μια μη επεμβατική και με δυνητικά μεγαλύτερη ακρίβεια εναλλακτική λύση στη συμβατική βιοψία ιστού, επιτρέποντας την έγκαιρη ανίχνευση, την παρακολούθηση της ανταπόκρισης στη θεραπεία και την εξατομικευμένη ιατρική. Οι μελέτες για τη δοκιμή της υγρής βιοψίας σε εναλλακτικά σωματικά υγρά εκτός του αίματος, όπως ούρα, υπεζωκοτική/ασκιτική συλλογή ή σάλιο, έχουν δώσει κάποια προκαταρκτικά αλλά πολλά υποσχόμενα στοιχεία ως προς την ένταξή τους στην καθημερινή κλινική πρακτική.
Η τεχνητή νοημοσύνη έχει πολλές κλινικές εφαρμογές και διαδραματίζει αναπόσπαστο ρόλο στη βιομοριακή έρευνα, με σαφείς προεκτάσεις στην ανάπτυξη της υγρής βιοψίας. Τα συστήματα τεχνητής νοημοσύνης μπορούν να συνυπολογίσουν τα αποτελέσματα πολλών βιοδεικτών ταυτόχρονα και να εντοπίσουν σχέσεις μεταξύ αυτών, κάτι που θα ήταν δύσκολο να πραγματοποιηθεί χρησιμοποιώντας παραδοσιακές προσεγγίσεις. Επιπλέον η μηχανική μάθηση έχει εφαρμοστεί για την ενσωμάτωση των αποτελεσμάτων της μοριακής υγρής βιοψίας σε κλινικά και απεικονιστικά δεδομένα ασθενών προκειμένου να βοηθηθούν οι θεραπευτικές αποφάσεις.
Είναι αναμφίβολο ότι η υγρή βιοψία δίνει μία νέα διάσταση στην ιατρική ακριβείας και αποτελεί ένα πολλά υποσχόμενο και επαναστατικό όπλο στα χέρια των σύγχρονων ιατρών Ογκολόγων. Στο ΙΑΣΩ Θεσσαλίας η υγρή βιοψία είναι εδώ και καιρό μέρος της καθημερινής κλινικής πρακτικής προσφέροντας στους ασθενείς μία από τις πιο σύγχρονες διαγνωστικές δυνατότητες.
Χριστόφορος Αστάρας MD–PhD
Παθολόγος Ογκολόγος
Διδάκτωρ Πανεπιστημίου Γενεύης Ελβετίας
Επιστημονικός Συνεργάτης Ά Κλινικής Παθολογικής Ογκολογίας ΙΑΣΩ Θεσσαλίας